根据van der Veen等人[7]描述的方法评估同质性。为了测试瓶间的同质性,从CRM AZA Mus的整个灌装系列中选择了15个单元,并通过LC-MS进行了测试[8]。为了检查瓶内的均匀性,在充分混合后,从一瓶CRM AZA Mus中均匀抽取四个子样品(见使用说明一节)。在重复性条件下对均匀性样品进行提取和LC-MS分析。由于CRM AZA Mus的瓶子之间的变化而产生的不确定性被推导出CRM AZA Mus的最终组合不确定性。
贻贝组织中的原多甲藻酸标准品CRM-AZA-Mus稳定性研究
CRM AZA-Mus的等时短期稳定性研究表明,AZA1、-2和-3在+18°C下两周内具有良好的稳定性。因此,在CRM的运输和运输过程中降解的风险有限。AZA1、-2和-3在-12°C的CRM AZA-Mus中具有良好的长期稳定性,在这种条件下的12个月内测量浓度没有显著变化。确定了与长期稳定性评估相关的不确定性,以纳入CRM AZA Mus的最终组合不确定性。
贻贝组织中的原多甲藻酸标准品CRM-AZA-Mus认证价值
AZA1、-2和-3的认证值(表1)是使用两种单独提取和定量方法的组合获得的[8]。第一种方法使用了详尽的液-固萃取方法,并伴有标准添加,以补偿LC-MS分析中的基质效应。在第二种方法中,使用穷举基质固相分散(MSPD)方法和基质匹配校准(MMC)提取CRM AZA-Mus,以说明LC-MS分析中的基质效应。使用生物毒素计量公司提供的AZA校准溶液制备用于标准添加的加标溶液:CRM-AZA1、-AZA2和-AZA3。对于MMC校准品,将CRM掺入“空白”贻贝组织(CRM Zero-Mus)提取物中,该提取物采用与CRM AZA-Mus相同的MSPD方法制备。
需要注意的是,AZA1、-2和-3的认证值是作为每个类似物的主峰和结构异构体的总和计算的,这些类似物稍后用用于我们测量的流动相柱系统洗脱(见图2)。对于一些更常用的流动相柱系统(见图3),异构体可能无法从主要的毒素类似物中分离出来。当结合主要AZA及其异构体的峰面积时,使用等摩尔响应因子。异构体峰面积对应于AZA1和AZA2的总峰的约10%,以及AZA3的总峰面积的约7%(数据未示出)。
不确定性
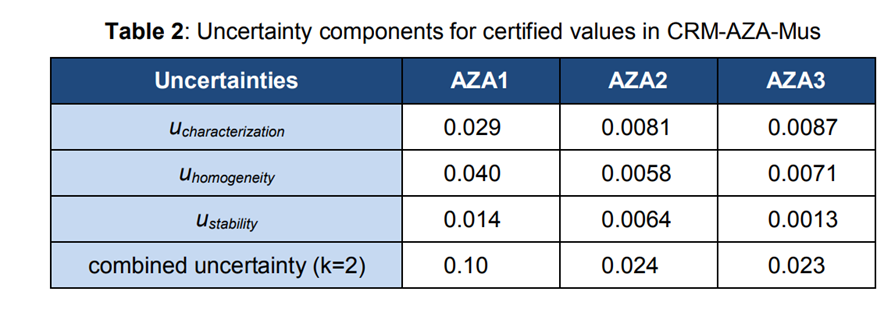
CRM AZA-Mus的总体不确定度估计(UCRM)包括与批次表征(uchar)、瓶间变化(uhom)和长期储存期间的不稳定性(ustab)相关的不确定性[9]。这些组件可以组合为:
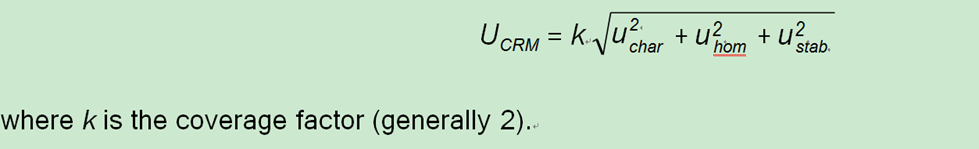
考虑了与CRM AZA Mus表征相关的所有误差来源。AZA1、-2和-3的认证值基于两种分析方法的组合。均匀性的不确定性(uhom)是整体不确定性的重要组成部分,因为CRM AZA Mus是一种基质材料。长期稳定性的不确定性(ustab)是根据CRM AZA-Mus的一年保质期计算的,而短期稳定性的不确定度没有考虑在内。将覆盖因子2应用于组合不确定度,从而得出最终标准不确定度值(表2)。应生物毒素计量局的要求,可提供CRM AZA Mus认证中应用的不确定度方法的详细说明。